Eine kurze Zusammenfassung
Eine runtergebrochene Erklärung der Überlegungen und Erkenntnisse aus meinem letzten Substack
Englische Autoübersetzung
Ein brillanter Physiker, dessen Expertise ich mehr als schätze, machte mich auf ein gravierendes Problem aufmerksam: Nicht jeder ist es gewohnt einen Prozess aus aktiven, logischen Überlegungen, die man aus Papers anstellen kann, zu folgen. Mein Substack ist eben eine solche aktive Überlegung, sprich ein erkenntnisgewinnender Prozess. Ich denke schnell und oft auch um drei Ecken schon 2 Schritte voraus.
Ich werde es also versuchen, noch einmal etwas umzustrukturieren und quasi eine “essentielle”-Zusammenfassung zu schreiben. (Die Papers findet ihr alle in meinem Hauptsubstack, seht es mir also nach, wenn ich nicht jedes noch einmal einzeln durchkaue und verlinke).
Die Kernaussage ist: L(ipid)N(ano)P(artikel)s [synthetisches Fettbombezeugs, in das die modRNA gepackt ist) penetrieren die phospholipide Doppelschicht und lösen hochinflammatorische Reaktionen aus + diverse Veränderungen(Alterationen) in der Genexpression(Expremierung)(Synthese von Proteine). Daraus ergibt sich eine logische Schlussfolgerungskette:
Zellmembranen sind unglaublich komplex strukturiert. Sie haben unzählige signalübertragungsauslösende (Signaltransduktion) Rezeptorproteine gebunden, welche in permanenter Bewegung sind. Zudem werden sie selbst von Signaltransduktionen in der Reorganisation nach der Endozytose (die Membran umschließt eine extrazelluläre Substanz und leitet diese in das Zytosol(Zellflüssigkeit) reguliert. Die LNPs sind synthetische Fettbomben, aus mehreren Lipiden bestehend. Wenn also sowohl NF-kB (ein Nuklearfaktor, sprich etwas in den Nukleus transportierend) als auch RAS als Signalprotein aktiviert waren, muss mind. eine Signalkette in den Kern gegangen sein. Da es jedoch über 8k Gene waren, die Alterationen in der Expression erfuhren, werden es mehr als nur eine Signalkaskade gewesen sein.
https://www.sciencedirect.com/science/article/pii/S0009308423000166
Einschub 05.03.2024
Wem dieses Paper zu theoretisch wäre und scheinbar ja nur eine Modellrechnung:
https://ascendiapharma.com/newsroom/2022/07/28/liposome-vs-lipid-nanoparticle
Zunächst: Der Unterschied zwischen “einfachen” Liposomen und den Lipidnanopartikelformulierungen der Schüsse läge in der Komplexität. Nicht aber in der Funktionsweise der einzelnen Komponenten.
The Structural Organization of Cationic Lipid-DNA Complexes*
https://sciencedirect.com/science/article/pii/S0005273607000764
Barriers and Strategies of Cationic Liposomes for Cancer Gene Therapy
Warum fand diese Tech wohl Anwendung in der Krebsforschung?
Einschub ende
https://www.cell.com/iscience/fulltext/S2589-0042(21)01450-4
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9936473/
Auch hier zeigten die Autoren die Aktivierung diverser Interleukine, Interferone und Aktivierung gereifter dendritischer Zellen nach der Behandlung mit leeren Lipiden. Dies lässt den Schluss zu, dass eine inflammatorische Reaktion statt fand.
Mit diesen Erkenntnissen ergab sich also zunächst die Frage, wie die phospholipide Doppelschicht überhaupt funktioniert, womit ich hier also noch einmal grob vereinfacht einsteigen möchte. Und eine weitere Frage, die mich umtrieb: Wie kam es überhaupt zu diesen Entzündungsreaktionen und Alterationen der Genexpression, sprich was und wie geht es in den Nukleus?
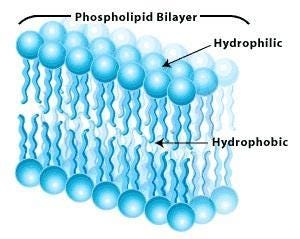
Die Phospholipide Doppelschicht (Membran) Besteht aus 2 Schichten von negativ geladenen Phospholipiden und Sphingolipiden (mit gesättigten und ungesättigten Acylketten gebunden) [wie dies aussieht entnehmt ihr der folgenden Schematik]. Es gibt hydrophobe (wasserabstoßende) und hydrophile (wasserliebende) Bereiche. Der Innenbereich der Membran (sprich die Schwanzteile) ist wasserabstoßend während die Phospholipide (der Kopf), zu den Flüssigkeiten gerichtet, diese anziehen.) Dies ermöglicht die Flexibilität und Beweglichkeit der Membran. Die Fluidität beschreibt dabei die Anpassung von Zellform an die Bewegung.
Hydrophil/hydrophob
Klären wir noch einmal die 3 hauptursächlichen Fluiditätsfaktoren (da das Lernvideo, welches ich verlinkte, recht lang ist.):
Temperaturabhängig: je höher desto beweglicher
Cholesterolabhängig: je höher die Konzentration desto weniger beweglich, da die Acetylketten (Fettsäureketten) stärker aneinander binden
Von der Actylkettensättigung abhängig: Ungesättigt (hohe Anzahl an Doppelbindungen) beweglicher (Fließfähigkeit erhöht), gesättigt weniger beweglich (steifer) (keine Doppelbindungen)
( https://pubmed.ncbi.nlm.nih.gov/17651712/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8002861/ )
Eine unbeantwortete Frage die sich schon alleine aus diesem Umstand ergibt: Wurde die Fluidität der Membran verändert, nach dem die Fettbomben reinkrachen?
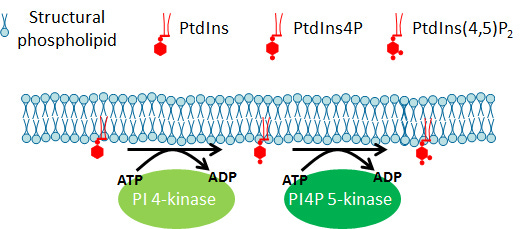
Des Weiteren finden sich Phosphoinositide (ungefähr 1%) in der Membran, die als regulatorische Lipide fungieren und phosphorylierte Derivate von Phosphatidylinositol (PtdIns) sind.
https://www.biochemtech.uni-halle.de/pflanze/2351734_2361571/
”Die Membranen eukaryotischer Zellen bestehen vorwiegend aus Strukturphospholipiden, enthalten jedoch auch geringe Anteile von Lipiden mit wichtigen regulatorischen Funktionen. Ein Beispiel für solche regulatorischen Lipide sind Phosphoinositide (PIs).”
Daraus resultiert zuallererst, bevor man sich dem Prozess der Penetration und sich daraus ergebenden Folgen stellen kann, die logische Frage: Wenn doch an der Membran all die Signalrezeptorproteine, wie VEGFR, EGFR, TLRs, SCAVENGER, just name one, hängen und außerdem Ionenkanäle verankert sind: Beeinflusst und wenn ja, wie, die Membran diese?
Hier die Kurzfassung aus meinem Substack an Erkenntnisgewinn:
Die Membran ist unglaublich komplex und ein echtes Wunderwerk. Sie wird von Signalkaskaden von unter anderem der MAPkkk/kk/k (Mitogen Aktivierende Protein Kinasen) über RAS reorganisiert via Interaktionen mit Effektorproteinen wie PI3K. Außerdem nimmt sie auch direkten Einfluss auf diese Signaltransduktionen. Diese Signalkaskaden sind stets stromabwärts (downstream) Richtung Nukleus gerichtet. (Ich führe dann recht detailliert aus, wie diese Mechanismen funktionieren, um die absolute Abhängigkeit der Signaltransduktion (Übertragung von extrazellulären Signalen in die Zelle zum Nukleus) und Membran in Wechselwirkung zu verdeutlichen.)
https://www.sciencedirect.com/science/article/abs/pii/S0169409X12001901
Und es war seit 2012 schon bekannt, dass kationische Lipide die Signaltransduktion aktivieren und alterieren.
Zusammenfassung:
Jede Endozytose löst zwingend downstream Signalkaskaden aus, da diese auch an der Reorganisation der Membran und deren Fluidität beteiligt sind. Kaskaden sind jedoch keine einzelnen Signale, sondern eine Kette von Signalen, die auch zur Genexpression führen, da sie ein Signal in den Nukleus transportieren. Daraus kann man also logisch ableiten, dass etwas mit diesen Kaskaden nach der Penetration passierte, was vielleicht nicht so toll ist, da wir bis heute noch nicht mal im Ansatz diese Mechanismen begriffen haben und falsche Signale unglaublichen Schaden anrichten können.
Im weiteren Substack zeige ich dann anhand von Beispielen, wie wenig wir wirklich über diese komplexen Interaktionen verstanden haben und erkläre anhand einiger Beispiele, wie solche Signaltransduktionen funktionieren. Ich zeige, dass sie sich stets in Crosstalks (das heißt Check und Ballance-Mechanismen, die aktivieren oder inhibieren[unterdrücken]), mit unzähligen anderen Signalkaskaden wie den beiden mTOR-Komplexen oder der Sonic Hedgehog-Kaskade befinden.
Eine schlüssige Überlegung die sich daraus ergibt: Wenn also RAS die Zellmembranreorganisation beeinflusst und direkt von der Phospholipidumgebung gesteuert wird und durch diese Fettbomben falsch getriggert wurde: Was passiert dann mit spike- oder eben auch nicht-spike exprimierenden Zellen, welche nicht zerstört werden? Es ist davon auszugehen, dass nicht jedes Lipid es in die Zelle mit endosomalen Escape (das heißt die modRNA wird ausgepackt) schaffte und auch nicht jedes Lipid die modRNA in sich trägt. Das Ende vom Lied wäre also eine völlig falsch aktivierte Zelle, durch falsche Eingangssignale aus der Bahn geworfen und das mal X, da wir nicht mal genau wissen, wie viele Lipide in den Schüssen stecken und wie viele davon leer waren. Noch dazu wäre die Frage, ob die Zellen wirklich so ohne weiteres zerstört würden, selbst wenn sie das Spikeprotein expremieren, da zu diesen ersten Prozessen noch die gesamten Translationsinteraktionen mit den Signalkaskaden und die Interaktionen des Spikeproteins als solches mit dazu addiert werden müssen. Wenn die Upstreamkonsequenzen (das heißt, wenn etwas in den Nukleus geht, löst es auch Reaktionen aus, die aus dem Nukleus zurück in die Zelle gehen) beispielsweise in einer Überexpressierung des Programmed Death Ligand 1 (PD-L1) münden, wie ich an einer aktuellen Studie im Substack zeige, ist es mehr als fraglich, ob diese Zellen überhaupt so ohne weiteres “sterben”.
Im Weiteren führe ich noch aus, was so alles schief gehen kann. Es ist meiner Meinung nach wichtig, zu verstehen, dass die Signaltransduktionswege an unzähligen Krankheiten, inklusive diverser Krebsarten, Autoimmunerkrankungen und neuronaler Krankheiten eine Schlüsselrolle spielen.
https://www.nature.com/articles/s41578-021-00358-0
https://pubmed.ncbi.nlm.nih.gov/35688311/
Ich muss gestehen, bei den Biodistributionsstudien, die ich auch in meinem langen Artikel diskutiere, habe ich ein wenig geschlampt: Es ist wichtig, zu verstehen, dass eine randomisierte Transfektionsrate und Verteilung über den ganzen Organismus statt findet, um zu verstehen, was alles schief gehen kann, mit falsch ausgelösten Signalkaskaden. Denn nicht jeder Zelltyp interagiert auf gleiche Art und Weise mit der MAPkkk/kk/k und all den anderen Signaltransduktionskaskaden und jede Interaktion hat unzählige mögliche Folgen. Von Maturation(Reifung) der dendritischen Zellen beispielsweise, über ganz spezifische Zytokinexpressierungen (was eben alles als Reaktion upstream folgt), bis hin zu Zellzyklusregulatoren wie den der cyclin dependent kinases (CDKs). Noch dazu ist es ganz schwer abzuschätzen, welche Zelltypen transfiziert wurden. Dendritische Zellen? Die Hersteller sprachen lediglich von Hostzellen. Diverse Studien zeigten die Transfektion von dendritischen Zellen. Dennoch kann man davon ausgehen, dass auch viele Endothel- und Epithelzellen transifiziert wurden.
Ein weiterer Kritikpunkt an meinem Susbtack ist dieser Satz:
Den muss ich wohl noch kurz erklären: Es geht um die zeitliche Verteilung der Fettbomben LNP: Je länger diese im System transportiert werden und sie nicht abgebaut werden, desto länger besteht die Möglichkeit, da sich die Fluidität der Membran verändern kann und noch mehr Zellen transfiziert werden. Was dann auch die RNA-Konzentrationszunahme >24 Stunden in diversen Organen erklären würde. Wenn die LNPs auch von der Sättigung der Membran abhängen und diese variieren kann, würde durch diese Variationen eventuell noch das ein oder andere LNP in die Membran krachen und das Elend beginnt von vorne.